| 摘要:依据Al(Ⅲ)、Zr(Ⅳ)的水解聚合机理,把锆、铝和钇的无机盐溶液按一定组成混合在一起,通过加入乙二醇作为络合剂和调节溶液的PH值来获得溶胶,并直接蒸馏溶胶来获得干凝胶,最后制得ZrO2(Y2O3)- Al2O3系粉末。研究结果表明:该工艺不仅制粉时间快、成本低、产量大,而且粒子均匀,粒径在20~50nm之间,具有一定的可行性。 关键词稀土,溶胶―凝胶法,水解―聚合,乙二醇 1 前言 化学法制备稀土稳定氧化锆超细粉末的工艺有机械法[1]、溶胶―凝胶法[2]、水解法[3]和溶剂蒸发分解法等[4]。其中尤以溶胶―凝胶法制得的粉末组成均匀,纯度高,颗粒细。但该方法制粉时间长,原料大都采用锆、铝的醇盐,价格昂贵。本实验首次采用非醇盐原料,通过加入乙二醇为络合剂,并调节酸度来获得溶胶,最后热处理制得Y2O3-ZrO2-Al2O3系超细粉末。 2 实验部分 试剂Y2O3纯度>99.9%,ZrOCl2.8H2O(CP),HCl(AR),HOCH2CH2OH(CP),AlCl36H2O(AR)。 Y2O3-ZrO2-Al2O3系超细粉的制备工艺流程如图1。 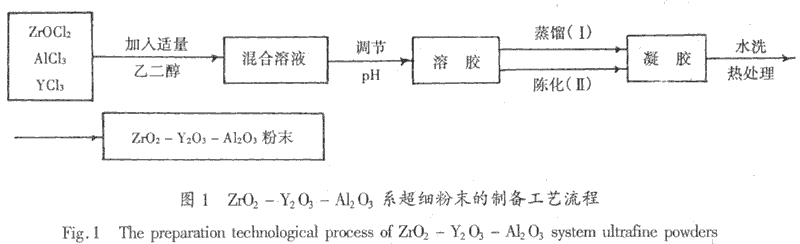
研究表明:水解温度越高,凝胶时间越短。对于符合快速聚沉动力学的体系。其粒子聚沉时间t与反应温度T成反比,这与实验结果相吻合,如图2(a)所示。在酸度与反应速度(h)的关系中,存在一个极值点(溶胶最稳定点),随着酸度的增大出现了最快胶凝点(胶体的等电点)。这时胶粒表面电荷正好全部中和,因而胶凝速度最快。说明Al(Ⅲ)和Zr(Ⅳ)的胶凝速度主要取决于溶胶的电化学性质,这符合Al(Ⅲ)、Zr(Ⅳ)的水解、聚合机理,如图2(b)所示。 3.3 凝胶的热分析 Y2O3-ZrO2-Al2O3凝胶的DTA、TGA曲线如图4。在200℃附近的吸热峰是由于乙二醇的挥发;在250℃以后添加剂发生分解,在380℃出现尖峰,为氧化锆凝胶转变成氧化锆结晶;在430℃附近的宽峰为无定形氧化铝向γ―Al2O3晶化所致。大部分重量的减少发生在500℃以下,在500℃以后的少量失重可能是由于残余碳的挥发。 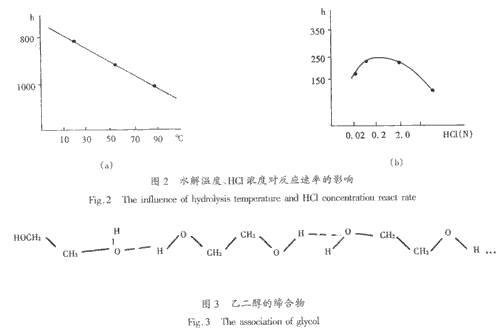
3.4 粉末的TEM电镜分析 由流程(Ⅰ)得到干凝胶,然后在1100℃下煅烧得到Y2O3-ZrO2-Al2O3粉末(图5)。从照片中可以看出,粒子接近等轴,且大小均匀,粒径在20~50mm之间。另外,粒子有些聚集,这是因为粒子很小,具有高的表面能。因此,在高温下容易烧结。 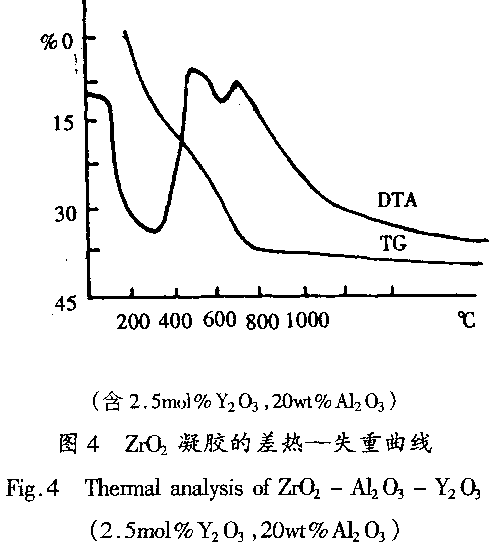
实验还表明,由流程(Ⅰ)制粉比流程(Ⅱ)可缩短2~3天时间(主要是凝胶时间),而且流程(Ⅰ)中乙二醇可回收利用,因此,该工艺具有可行性。 3.5 粉末的XRD分析和稀土Y2O3的稳定作有 (1) Zr(Ⅳ)离子(0.82A)的晶格尺寸和Y(Ⅲ)离子(0.88A)的晶格尺寸之间差别很小;(2)锆的电负性(1.33)与钇的电负性(1.22),以及Zr(Ⅳ)和Y(Ⅲ)之间的电荷差别均较小;(3)Y2O3比ZrO2有较多的共价异极连续,因此Y2O3成功用于ZrO2陶瓷从四方晶系转变到单斜晶系时的稳定剂[5]。本实验的X-射线图谱表明(图6),在Y2O3的稳定作用下,ZrO2大都以介稳四方相存在,图中出现了少量的单斜相ZrO2,可能是因为锻烧温度太高(1100℃),接近四方一单斜的相变温度(1170℃),部分大粒径的ZrO2超过介稳四方相存在的临界尺寸,相变成稳定的单斜相。 (2)  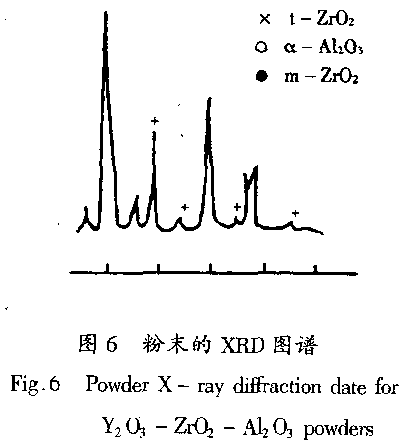
3.6 Al(Ⅲ)和Zr(Ⅳ)的水解聚合机理 对于Zr(Ⅳ)、Al(Ⅲ)的混合溶液,其水解和凝聚与溶液的酸度有密切的关系。当两种原子混合时,将发生部分电荷的传递,并在一定条件下,减少酸度并发生如下反应[6]:  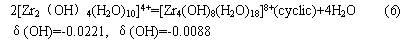 与此同时,阴离子在上述水解和聚合过程中起着非常重要的作用,酸性催化剂能够直接影响它的凝胶性能(如图2(b))。 Livage等人[7]研究表明:阴离子能够协调Al3+和Zr4+系统在酸性介质中的溶解聚合。其典型的Al3+和Zr4+的介质有:[Al(X)(OH2)4]2+和[Al(OH)(HX)(H2O)3]2+;[Al2(X)(OH)2(OH2)6]3+和[Al2(X)(OH)3(OH2)5]3+;[Zr(X)(H2O)6]3+和[Zr(OH)(HX)(OH2)5]3+;[Zr(X)(OH2)(OH2)4]1+和[Zr(HX)(OH3)(H2O)3]1+等,式中X=Cl-等。 因此,在含Cl-阴离子的Al(Ⅲ)和Zr(Ⅳ)液液中,通过调节溶液的酸度来控制溶液的水解和聚合速率是可行的。 4 结论 (1)含有Cl-阴离子的Al(Ⅲ)和Zr(Ⅳ)溶液,其水解和聚合速率依赖于溶胶的酸度和电学性质。 (2)乙二醇的作用机制表现为空间位阻效应。 (3)稀土Y2O3对ZrO2具有稳定作用,本研究表明,稀土稳定氧化锆超细粉末的合成工艺具有一定的可行性。
|

